Этиленгликоль
Содержание:
- Особенности Триэтиленгликоля (ТЭГ)
- Производство
- Пропиленгликоль или этиленгликоль: сравнение теплоносителей
- Применение [ править | править код ]
- Меры безопасности [ править | править код ]
- Важнейшие требования ГОСТ 19710 к готовому гликолю
- В чем разница G12 и G11, G12 и G13
- Область применения и цена. Этиленгликоль как антифриз, теплоноситель и охлаждающая жидкость в одном растворе
- Преимущества и недостатки
- Как можно отравиться?
- Области применения и ценовая политика продукционного ряда
- Применение этиленгликоля
- Теплоноситель – основные требования в системе отопления
Особенности Триэтиленгликоля (ТЭГ)
Стоит повторить, что данное вещество представляет собой бесцветную жидкость. Получают ее в процессе изготовления других отдельных химических веществ – этиленгликоля и диэтиленгликоля. Другими словами, данный раствор является продуктом побочного выхода.
Существует две основных марки триэтиленгликоля, которые отличаются содержанием процента ТЭГ:
- А марка – содержание ТЭГ 98%, в составе есть доля альдегидов, а также кислот;
- Б марка – содержание ТЭГ 90%.
Плотность соединения варьируется в пределах от 1,121 до 1,124 г/см. куб. Данная разница напрямую зависит от марки вещества. Химические свойства ТЭГа крайне схожи с характеристиками диэтиленгликоля. Температура плавления соединения равна -5оC, а температура кипения – 278,3оC.
Большая часть этилена расходуется на создание окиси этилена, производство которой систематически расширяется. Из-за высокой способности данного вещества к реакции из него получают целый список ценных химических соединений. Среди них важнейшими являются этиленгликоль, используемый во многих химических процессах, ди- и триэтиленгликоли, эфиры гликоля, этанол-амины и др.
Производство
Промышленные маршруты
Этиленгликоль получают из этилена (этена) через промежуточный оксид этилена . Оксид этилена реагирует с водой с образованием этиленгликоля в соответствии с химическим уравнением :
- С 2 Н 4 О + Н 2 О → НО-СН 2 СН 2 -ОН
Эта реакция может быть катализируемой с помощью либо кислот или оснований , или может иметь место при нейтральном значении рН при повышенных температурах. Наибольший выход этиленгликоля происходит при кислом или нейтральном pH с большим избытком воды. В этих условиях можно достичь выхода этиленгликоля 90%. Основными побочными продуктами являются олигомеры диэтиленгликоль , триэтиленгликоль и тетраэтиленгликоль . Разделение этих олигомеров и воды требует больших затрат энергии. Ежегодно производится около 6,7 млн тонн.
Более высокая селективность достигается за счет использования Shell «ы процесса OMEGA . В процессе OMEGA оксид этилена сначала превращается в диоксид углерода ( CO2) до этиленкарбоната . Затем это кольцо гидролизуют основным катализатором на второй стадии с получением моноэтиленгликоля с селективностью 98%. На этом этапе снова выделяется диоксид углерода, который может быть снова подан в технологический контур. Углекислый газ частично поступает из производства окиси этилена, где часть этилена полностью окисляется .
Этиленгликоль производится из окиси углерода в странах с большими запасами угля и менее строгими экологическими нормами. Окислительное карбонилирование метанола до диметилоксалата обеспечивает многообещающий подход к производству этиленгликоля на основе C 1 . Диметилоксалат может быть преобразован в этиленгликоль с высокими выходами (94,7%) путем гидрирования с медным катализатором:
Поскольку метанол перерабатывается, потребляются только окись углерода, водород и кислород. Один завод производственной мощностью 200 000 тонн этиленгликоля в год находится во Внутренней Монголии , а второй завод в китайской провинции Хэнань с мощностью 250 000 тонн в год был запланирован на 2012 год. По состоянию на 2015 год, четыре завода в Китае с производительностью 200 000 т / год каждая действовала, и, по крайней мере, еще 17 машин в будущем.
Биологические маршруты
У гусеницы большой восковой моли, Galleria mellonella , есть кишечные бактерии, способные разлагать полиэтилен (PE) до этиленгликоля.
Исторические маршруты
Согласно большинству источников, французский химик Шарль-Адольф Вюрц (1817–1884) впервые получил этиленгликоль в 1856 году. Сначала он обработал «иодид этилена» (C 2 H 4 I 2 ) ацетатом серебра, а затем гидролизовал полученный «диацетат этилена». с гидроксидом калия . Вюрц назвал свое новое соединение «гликоль», потому что он разделяет качества как этилового спирта (с одной гидроксильной группой), так и глицерина (с тремя гидроксильными группами). В 1859 году, Вюрец готовил этиленгликоль через гидратацию из окиси этилена . По всей видимости, до Первой мировой войны этиленгликоль не производился и не применялся в коммерческих целях , когда он был синтезирован из этилендихлорида в Германии и использовался в качестве заменителя глицерина во взрывчатых веществах .
В Соединенных Штатах полукоммерческое производство этиленгликоля через этиленхлоргидрин началось в 1917 году. Первый крупномасштабный промышленный завод по производству гликоля был построен в 1925 году в Южном Чарльстоне, Западная Вирджиния , компанией Carbide and Carbon Chemicals Co. (ныне Union Carbide Corp.) . К 1929 году этиленгликоль использовался почти всеми производителями динамита . В 1937 году компания Carbide запустила первую установку, основанную на процессе Лефорта, для парофазного окисления этилена до окиси этилена. Carbide сохраняла монополию на процесс прямого окисления до 1953 года, когда процесс научного проектирования был коммерциализирован и предложен для лицензирования.
Пропиленгликоль или этиленгликоль: сравнение теплоносителей
Пропиленгликоль и этиленгликоль (этандиол-1,2) – это простейшие двухатомные спирты, получившие широкую популярность, наряду с глицерином, в качестве низкозамерзающих жидкостей (антифризов) в системах отопления.
Их отличает от других теплоносителей то, что они прекрасно выдерживают высокие температуры при соединении с водой и начинают закипать только при 105°С-110°С при нормальном атмосферном давлении и при 120°С-150°С – при повышенном. В зависимости от степени разведения, температура их кристаллизации составляет от -40°С до -70°С.
В их составе могут присутствовать антикоррозионные присадки для защиты внутренних элементов системы от коррозии и снижения пенообразования, что позволяет существенно увеличить ее срок эксплуатации.
Отличие этиленгликоля от пропиленгликоля
Тепло- и хладоносители на основе этилен гликоля (этандиола) отличаются более высокими теплоемкостью и теплопроводностью по сравнению с водными растворами монопропиленгликоля, а это позволяет применять в схемах радиаторы и теплообменники меньшего размера. Они также обладают более низкой вязкостью, что обеспечивает лучшую циркуляцию теплоносителя внутри системы и снижение гидродинамических потерь.
Благодаря малой вязкости этандиола на его основе можно создавать растворы различных концентраций с максимально низкой температурой кристаллизации -70°С. При этом есть еще и главное отличие – этиленглико ль стоит почти в 2 раза дешевле своего конкурента.
Существенный недостаток этиленгликолевых растворов – их токсичность. Недопустимо их проникновение в грунтовые воды и в почву, особенно в местах, где используется грунтовая вода и выращиваются сельскохозяйственные культуры.
При неосторожном применении антифриз может попасть внутрь организма, что способно привести к летальному исходу. Материал также обладает сладковатым вкусом и не имеет неприятного запаха, а это создает повышенную опасность для животных и детей в случае протечек
Материал также обладает сладковатым вкусом и не имеет неприятного запаха, а это создает повышенную опасность для животных и детей в случае протечек.
Пропиленгликоль или этиленгликоль в отоплении?
Водные растворы пропилен гликоля не обладают токсичностью и подходят для использования в отопительных системах с высокими требованиями к экологичности: общественные и жилые постройки, фармацевтические, парфюмерные, косметические, пищевые производства и прочее. В таких инженерных схемах необходимо соблюдение экологической безопасности из-за риска проникновения антифриза в производимую продукцию и в производственные помещения.
Монопропиленгликоль предпочтителен для применения в системах отопления частных домов, коттеджных поселков, в местах, где используются грунтовые воды, почва или грунт для садов и огородов, сельскохозяйственных производств при опасности заражения продуктов и воды.
Несмотря на то, что по сравнению с этандиолом пропилен гликоль обладает большей вязкостью, теплоносители на его основе имеют «смазывающее» действие, улучшают функционирование насосов во вторичном контуре и способствуют удалению отложений с внутренних поверхностей теплообменного оборудования.
Этиленгликоль и пропиленгликоль: сравнение и выводы
Обобщив все вышесказанное, можно сделать вывод, что более высокие теплопроводность и теплоемкость этиленгликоля при его меньшей вязкости и доступной цене делают его предпочтительнее растворам на основе монопропиленгликоля. Но! Это правило действует только в тех случаях, где отсутствуют особые требования к экологичности теплоносителя.
Во всех остальных ситуациях необходимо использовать пропиленгликоль. Его отличия по теплофизическим свойствам от конкурента не столь существенны, но стоит он дороже. Хотя в данном случае это вопрос безопасности, на которой непозволительно экономить.
Теплоноситель этиленгликоль и пропиленгликоль: можно ли смешивать?
В связи с такой разницей в степени токсичности и в цене у многих возникает вопрос: можно ли смешать два спирта, чтобы получить не такой дорогой, как монопропиленгликоль, но менее токсичный, чем этандиол, аналог?
Ответ категоричен: жидкости не подлежат смешиванию, так как это, в лучшем случае, может привести к снижению характеристик более технологичного состава – пропилен гликоля, а в худшем вызовет образование осадка, так как растворы могут содержать присадки, несовместимые между собой. Поэтому следует выбрать только один из антифризов в соответствии с требованиями системы, а купить их по выгодным ценам можно у нас.
Применение [ править | править код ]
Благодаря своей дешевизне этиленгликоль нашёл широкое применение в технике.
- Как компонент автомобильных антифризов и тормозных жидкостей, что составляет 60% его потребления. Смесь 60% этиленгликоля и 40% воды замерзает при −49 °С. Коррозионно активен, поэтому применяется с ингибиторами коррозии;
- Используется как теплоноситель с содержанием не более 50% в системах отопления (частные дома в основном)
- В качестве теплоносителя в виде раствора в автомобилях, в системах жидкостного охлаждения компьютеров;
- В производстве целлофана, полиуретанов и ряда других полимеров. Это второе основное применение;
- Как растворитель красящих веществ;
- В органическом синтезе:
- в качестве высокотемпературного растворителя.
- для защиты карбонильной группы путём получения 1,3-диоксолана. Обработкой вещества с карбонильной группой в бензоле или толуоле этиленгликолем в присутствии кислого катализатора (толуолсульфоновой кислоты, BF3•Et2O и др.) и азеотропной отгонкой на насадке Дина-Старка образующейся воды. Например, защита карбонильной группы изофорона
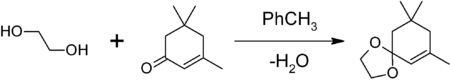
1,3-диоксоланы могут быть получены также при реакции этиленгликоля с карбонильными соединениями в присутствии триметилхлорсилана или комплекса диметилсульфат-ДМФА 1,3-диоксалана устойчивы к действию нуклеофилов и оснований. Легко регенерируют исходное карбонильное соединение в присутствии кислоты и воды.
- Как компонент противоводокристаллизационной жидкости «И».
- В качестве криопротектора.
- Для поглощения воды, для предотвращения образования гидрата метана (ингибитор гидратообразования), который забивает трубопроводы при добыче газа в открытом море. На наземных станциях его регенерируют путём осушения и удаления солей.
- Этиленгликоль является исходным сырьём для производства взрывчатого веществанитрогликоля.
Этиленгликоль также применяется:
- при производстве конденсаторов
- при производстве 1,4-диоксана
- как теплоноситель в системах чиллер-фанкойл
- в качестве компонента крема для обуви (1‒2 %)
- в составе для мытья стёкол вместе с изопропиловым спиртом
- при криоконсервировании биологических объектов (в крионике) в качестве криопротектора.
- при производстве полиэтилентерефталата, пластика популярных ПЭТ-бутылок.
Меры безопасности [ править | править код ]
Этиленгликоль — горючее вещество. Температура вспышки паров 120 °C. Температура самовоспламенения 380 °C. Температурные пределы воспламенения паров в воздухе, °С: нижний — 112, верхний — 124. Пределы воспламенения паров в воздухе от нижнего до верхнего, 3,8‒6,4% (по объему).
Этиленгликоль умеренно токсичен . По степени воздействия на организм относится к веществам 3-го класса опасности.
Летальная доза при однократном пероральном употреблении составляет 100‒300 мл этиленгликоля (1,5‒5 мл/кг массы тела) . Имеет относительно низкую летучесть при нормальной температуре, пары обладают не столь высокой токсичностью и представляют опасность лишь при хроническом вдыхании. Определённую опасность представляют туманы, однако при их вдыхании об опасности сигнализируют раздражение и кашель. Противоядием при отравлении этиленгликолем являются этанол и 4-метилпиразол .
В организме метаболизируется путём окисления до альдегида гликолевой кислоты и далее до гликолевой кислоты, которая затем распадается до муравьиной кислоты и диоксида углерода. Также он частично окисляется до щавелевой кислоты, которая вызывает повреждения почечной ткани. Этиленгликоль и его метаболиты выводятся из организма с мочой .
Самые известные и применяемые в жизни человека и в промышленности вещества, принадлежащие к категории многоатомных спиртов – это этиленгликоль и глицерин. Их исследование и использование началось несколько веков назад, но свойства этих органических соединений во многом неповторимы и уникальны, что делает их незаменимыми и по сей день. Многоатомные спирты используют во многих химических синтезах, отраслях промышленности и сферах человеческой жизнедеятельности.
Важнейшие требования ГОСТ 19710 к готовому гликолю
С 1984 года действует ГОСТ 19710, который устанавливает требования к тому, какие свойства (температура замерзания, плотность и так далее) должен иметь этиленгликоль, используемый на предприятиях автомобилестроения и в других отраслях народного хозяйства, где на его основе выпускают разнообразные составы.
По ГОСТ 19710 гликоль (как жидкость) может быть двух типов: первого сорта и высшего сорта. Доля (массовая) воды в гликоле первого сорта должна быть до 0,5 %, высшего – до 0,1 %, железа – до 0,00005 и 0,00001 %, кислот (в пересчете на уксусную кислоту) – до 0,005 и 0,0006 %. Остаток после прокаливания готового продукта не может быть более 0,002 и 0,001 %.

Цвет 1,2-диоксиэтана по ГОСТ 19710 (по шкале Хазена):
- после кипячения в растворе кислоты (соляной) – 20 единиц для продукции высшего сорта (первый сорт не нормируется по цвету);
- в стандартном состоянии – 5 (высший сорт) и 20 единиц (первый сорт).
В Государственном стандарте 19710 выдвигаются специальные требования к процессу производства описываемого простейшего спирта:
- используется исключительно герметичная аппаратура и оборудование;
- производственное помещение обязательно оснащается вентиляцией, рекомендованной для работы с соединениями, которым присвоен третий класс опасности;
- при попадании гликоля на оборудование или землю его следует сразу же обильно смывать водной струей;
- персонал, работающий в цеху по производству 1,2-этандиола, обеспечивается противогазом модели «БКФ» либо иным приспособлением для защиты органов дыхания, соответствующим ГОСТ 12.4.034;
- возгорания гликоля тушат при помощи инертных газов, специальных пенных составов, а также тонкораспыленной воды.

Готовая продукция по ГОСТ 19710 проверяется различными методами. Например, массовая часть двухатомного спирта и диэтиленгликоля устанавливается способом изотермической газовой хроматографии по технологии так называемого «внутреннего эталона». При этом используются весы для лабораторных исследований (ГОСТ 24104), стеклянная или стальная газохроматографическая колонка и хроматограф с детектором ионизационного типа, измерительная линейка, микрошприц, лупа оптическая (ГОСТ 25706), выпарительная чашка и другой инструмент.
Цвет гликоля устанавливают по стандарту 29131 при помощи секундомера, специального цилиндра, конической колбы, соляной кислоты, холодильного агрегата. Массовая часть железа устанавливается по Госстандарту 10555 по методике сульфациловой фотометрии, остатка после прокаливания – по Госстандарту 27184 (посредством выпаривания полученного соединения в платиновой либо кварцевой емкости). А вот массовая часть воды определяется электрометрическим или визуальным титрованием с использованием реактива Фишера в бюретках емкостью 10 либо 3 кубических сантиметра.
В чем разница G12 и G11, G12 и G13
Основные виды антифризов, такие как G11, G12 и G13 отличаются по виду используемых присадок: органические и неорганические.
Общие сведения об антифризах, в чем между ними отличие и как подбирать нужную ОЖ
Охлаждающая жидкость класса G11 неорганического происхождения с малым набором присадок, наличием фосфатов и нитратов. Такой антифриз создан по силикатной технологии. Силикатные присадки покрывают внутреннюю поверхность системы сплошным защитным слоем в не зависимости от наличия участков коррозии. Хотя такой слой и защищает уже существующие очаги коррозии от разрушений. Такой антифриз имеет низкую стабильность, ухудшенную теплоотдачу и небольшой строк эксплуатации, после выработки, которого, выпадает в осадок, образовывающий абразив и повреждающий тем самым .
Через то, что антифриз G11 создает слой подобный накипи в чайнике, он не подходит для охлаждения современных авто, имеющих радиаторы с тонкими каналами. К тому же, температура кипения такой охлаждайки составляет 105 °С, а строк службы не более 2-х лет или 50-80 тыс. км. пробега.
Зачастую антифриз G11 окрашивается в зеленый или синий цвета. Такую ОЖ применяют для автомобилей, выпущенных до 1996 года и машины с большим объёмом охлаждающей системы.
G11 плохо подходит к алюминиевым радиаторам и блокам, так как его присадки не могут должным образом защищать этот металл при высоких температурах.
В Европе авторитетная спецификация классов антифризов принадлежит концерну Volkswagen поэтому соответствующая маркировка VW TL 774-C предусматривает использование в антифризе неорганических присадок и имеет обозначение G 11. Спецификация VW TL 774-D предусматривает наличие карбо-кислотных добавок на органической основе и маркируется как G 12. Стандартами VW TL 774-F и VW TL 774-G маркируются классы G12 + и G12 ++, а самый сложный и дорогостоящий антифриз G13 регламентируется стандартом VW TL 774-J. Хотя другие производители такие как Форд или Тойота имеют свои стандарты качества. Кстати разницы между тосолом и антифризом нету. Тосол – одна из марок русского минерального антифриза, которая не рассчитан на работу в моторах с алюминиевым блоком.
Органические и неорганические антифризы смешивать категорически нельзя, поскольку возникнет процесс свертывания и в результате появится осадок в виде хлопьев!
А жидкости классов G12, G12 + и G13 разновидности органических антифризов «Long Life». Применяются в системах охлаждения современных авто выпускаемых начиная с 1996 г. G12 и G12 + на основе этиленгликоля но только G12 plus предполагает использование гибридной технологии производства в которой объединили силикатную технологию с карбоксилатную. В 2008 году появился еще и класс G12++, у такой жидкости, органическая основа сочетается с небольшим количеством минеральных присадок (называется лобридной Lobrid или SOAT coolants). У гибридных антифризах органические присадки смешиваются вместе с неорганическими (могут применяться силикаты, нитриты и фосфаты). Такое объединение технологий дало возможность устранять главный недостаток антифриза G12 – не только устранять коррозию, когда она уже появилась, но и выполнять профилактическое действие.
G12+, в отличии от G12 или G13 может быть смешана с жидкостью класса G11 или G12, но все равно такой «микс» не рекомендован.
Охлаждающая жидкость класса G13 начала производится с 2012-го и рассчитана для автомобильных двигателей работающих в экстремальных режимах. С технологической точки зрения отличий от G12 не имеет, единственная разница в том, что сделана на пропилен гликоле, который менее ядовитый, быстрее разлагается, а значит, наносит меньший вред окружающей среде при его утилизации и его цена значительно выше G12-го антифриза. Изобретался исходя из требований к повышению экологических норм. Антифриз G13, как правило, фиолетового или розового цвета, хотя на самом деле может окрашиваться любым цветом, так как это всего лишь краситель, от которого её характеристики не зависят, разные производители могут выпускать ОЖ с разными цветами и оттенками.
Разница в действии карбоксилатного и силикатного антифризов
Область применения и цена. Этиленгликоль как антифриз, теплоноситель и охлаждающая жидкость в одном растворе
Чудодейственных двухатомный спирт применяется очень широко, в огромном количестве отраслей и в повседневной жизни встречается куда чаще, чем может показаться – от науки и химической промышленности (органический синтез) до более привычных вещей – жизненно необходимых любому водителю антифриза, тормозных жидкостей, при производстве целлофана, моющих средств и даже обувных кремов. Применение этиленгликоля безусловно удобно и окупает себя.
Производство этиленгликоля дело требует минимальных затрат, а поэтому и себестоимость, и цена оптом (а в других целях, кроме промышленного использования, закупать этиленгликоль в чистом виде не имеет большого смысла) весьма демократична – поставщики запрашивают за килограмм продукта чуть больше пятидесяти рублей и всё будет зависеть от доли воды раствора и количества).
Так, за двадцать килограмм придётся заплатить полторы тысячи, а за двести сорок – почти шестнадцать тысяч рублей. Для особо бережливых покупателей есть предложения заливке вещества в вашу тару, поэтому и цену можно регулировать исходя из потребности.
Антифризы с этиленгликолем (примерно 5 килограмм) от производителей Sintec или Sibiria встанут автовладельцам в зависимости от состава и веса в суммы от ста до восьмисот рублей.
Преимущества и недостатки
Пропиленгликоль один из самых востребованных готовых теплоносителей для отопительных систем. Основной его функцией является защита оборудования обогрева от разрывов, что происходит благодаря способности практически не изменять свой объем при низких температурах. Поэтому в сильные морозы при его использовании нет необходимости слива системы.
К преимущественным сторонам применения теплоносителя на основе пропиленгликоля относят:
- Безопасность и экологичность. Вещество не содержит компонентов повышенной токсичности. Реактив не оказывает негативного воздействия при попадании на кожный покров или слизистую глаз. Его пары достаточно безвредны. При попадании на поверхность отделочного материала пола исключаются, какие либо химические реакции.
- Отсутствие коррозийной активности. Такое свойство позволяет применять данный теплоноситель для отопительных систем с различными конструктивными материалами.
- Высокий уровень теплофизических характеристик. Применение водного раствора пропиленгликоля для отопительных контуров способствует быстрому и равномерному нагреву помещения. При этом тепло удерживается достаточно долго.
- Отсутствие накипи. При нагревании до высоких температур данный антифриз не образует никаких твердых отложений. В то же время пропиленгликоль имеет бактерицидные и чистящие свойства. С его помощью удаляются различные налеты на внутренних участках отопительного оборудования.
Готовый раствор пропиленгликоля совершенно пожаробезопасный и его применение исключает возможность взрыва.
Данный теплоноситель также имеет некоторые отрицательные эксплуатационные моменты:
- Высокий показатель текучести. Пропиленгликоль способен проникать через самые незначительные щели. Его текучесть несколько выше от воды, поэтому иногда возникают протечки в местах, где их не должно быть. Но это свойство в тоже время можно отнести к положительным сторонам, так как позволяет улучшить качества сборки теплопроводной конструкции.
- Исключается возможность использование теплоносителя пропиленгликоль при наличии деталей, вмещающих цинк. Если не следовать такому предостережению, то вязкий антифриз со временем станет отслаивать оцинковку, что приведет к закупорке трубопровода.
Также иногда к отрицательным сторонам относят высокую стоимость антифриза на основе пропиленгликоля. При этом требуется его замена в системе отопления не реже чем через пять сезонов.
Как можно отравиться?
Этиленгликолем можно отравиться двумя способами:
- При вдыхании его паров;
- При употреблении внутрь;
- Через кожные покровы.
Попадание через дыхательные пути случается, как правило, на производстве в результате аварии, нарушения технологии производства и несоблюдения индивидуальных мер защиты. Этиленгликоль очень летуч, поэтому высокой концентрации в воздухе практически не создается, а отравления таким путем носят хронический характер – периодическое вдыхание небольших доз паров вещества.
 Другой, наиболее опасный и частый путь отравления – прием вещества внутрь. Это может быть случайно, когда этиленгликоль хранится в бутылке из-под напитков, или оставлен в доступном для детей месте. Но чаще всего подобные отравления случаются с людьми с алкогольной зависимостью, которые умышленно принимают его для опьянения.
Другой, наиболее опасный и частый путь отравления – прием вещества внутрь. Это может быть случайно, когда этиленгликоль хранится в бутылке из-под напитков, или оставлен в доступном для детей месте. Но чаще всего подобные отравления случаются с людьми с алкогольной зависимостью, которые умышленно принимают его для опьянения.
С этой целью его также получают в домашних условиях путем перегонки через аппарат-дистиллятор антифриза или тормозной жидкости. Отсутствие какого-либо запаха и сладковатый привкус вводят в заблуждение, что этот «аналог» этилового спирта не опасен, что и приводит к передозировке.
Попадание через кожные покровы встречается довольно редко, только при длительном прямом контакте с жидкостью, при этом интоксикация бывает не сильно выражена.
Области применения и ценовая политика продукционного ряда
Стоимость на заводах и предприятиях, занимающихся производством и продажей подобных реактивов, колеблется в среднем около 100 рублей за килограмм такого химического соединения, как этиленгликоль. Цена зависит от чистоты вещества и максимального процентного содержания целевого продукта.

Применение этиленгликоля не ограничивается какой-то одной областью. Так, в качестве сырья его используют в производстве органических растворителей, искусственных смол и волокон, жидкостей, замерзающих при отрицательных температурах. Он задействован во многих промышленных отраслях, таких как автомобильная, авиационная, фармацевтическая, электротехническая, кожевенная, табачная. Неоспоримо весомо его значение для органического синтеза.
Важно помнить, что гликоль – это токсичное соединение, которое может нанести непоправимый вред здоровью человека. Поэтому его хранят в герметичных сосудах из алюминия или стали с обязательным внутренним слоем, защищающим ёмкость от коррозии, только в вертикальных положениях и помещениях, не снабженных отопительными системами, но с хорошей вентиляцией
Срок – не более пяти лет.
Применение этиленгликоля
Этиленгликоль широко применяется в химической и фармацевтической, в текстильной и электротехнической, в автомобильной и авиационной промышленностях.
Водные растворы этиленгликоля (незамерзающие жидкости) кристаллизуются (замерзают) при достаточно низких температурах, поэтому очень широко применяются в качестве теплоносителя (антифриза, хладагента) в автономных отопительных системах и в системах промышленного кондиционирования общественных зданий и спортивных сооружений, различных производств, где технологически требуется поддержание в помещениях необходимой низкой температуры. При кристаллизации-замерзании водный раствор этиленгликоля принимает форму мягкой желеобразной массы(!), исключая при этом вероятность повреждения оборудования отопительной системы или системы промышленного кондиционирования. В зависимости от климатических режимов работы оборудования применяются теплоносители на основе водных растворов с содержанием 30%, 36%, 40%, 45%, 50%, 54% и 65% этиленгликоля, с рабочим диапазоном температур до -15°C, -20°C, -25°C, -30°C, -35°C, -40°C и -65°C соответственно и с антикоррозионными, противонакипными и противопенными присадками.
Водный раствор этиленгликоля при одной и той же концентрации имеет более низкую температуру кристаллизации (замерзания) по сравнению с водными растворами на основе пропиленгликоля. Также раствор этиленгликоля по сравнению с растворами пропиленгликоля имеет более низкую вязкость, что существенно снижает потери при циркуляции раствора этиленгликоля в системе отопления (охлаждения, кондиционирования). Раствор этиленгликоля обладает и более высокими значеними теплоемкости и теплопроводности, поэтому ему и отдается предпочтение как теплоносителю (антифризу,хладагенту) в закрытых инженерных системах.
Важнейшим теплофизическим параметром водного раствора этиленгликоля является зависимость температуры замерзания раствора от его концентрации. Эта зависимость носит нелинейный характер и температура замерзания (кристаллизации) водного раствора достигает своего минимума в -65°C при концентрации 65%, затем при дальнейшем повышении концентрации до 98% температура замерзания повышается до -13°C. Концентрация, количество этиленгликоля, содержащегося в теплоносителе, формирует в основном и цену самого теплоносителя. Поэтому не целесообразно и экономически не выгодно производство и применение водных растворов с концентрацией выше 70%.
Нелинейный характер зависимости температуры кристаллизации водного раствора этиленгликоля от его концентрации представлены в табл. №1 в виде двух функциональных зависимостей: 1) значения величины плотностиводного раствора в зависимости от его концентрации при температуре 20°C и 2) зависимость температуры кристаллизации водного раствора от концентрациии этиленгликоля.
Табл. №1. Влияние концентрации этиленгликоля на температуру кристаллизацию водного раствора этиленгликоля. Значения (величины) плотности раствора при температуре 20°C.
| Концентрация этиленгликоля, % | Температура замерзания, °C | Плотность при 20 °C |
| 30% | -15 °C | 1,038 |
| 35% | -20 °C | 1,045 |
| 40% | -25 °C | 1,052 |
| 45% | -30 °C | 1,058 |
| 50% | -35 °C | 1,064 |
| 54% | -40 °C | 1,071 |
| 60% | -50 °C | 1,077 |
| 65% | -65 °C | 1,083 |
| 70% | -60 °C | 1,088 |
Теплоноситель – основные требования в системе отопления
Какой же должен быть теплоноситель для системы автономного отопления? Попробуем сформулировать необходимые критерии соответствия «идеального» варианта.
- Начнем с того, что жидкость на отопление нам понадобится с максимально высокой теплоемкостью. Это условие необходимо для качественного аккумулирования и дальнейшей отдачи тепловой энергии посредством радиаторов.
- Нам понадобится теплоноситель, с химическим составом не активизирующим коррозионные процессы в котельном оборудовании, в разводке труб, отопительно-радиаторных, запорно-регулирующих и прочих конструкциях отопительной системы.
- Особые требования следует выдвигать к химической составляющей теплоносителя. Состав проходит через уплотнения насосного оборудования, и другие конструктивные элементы содержащие резиновые уплотнительные кольца и может подвергать их к разрушению.
- Одним из главных показателей, указывающих, что у вас в распоряжении качественный теплоноситель — широкий диапазон температурного использования. Производитель заботящийся о своей репутации предлагает теплоноситель с рабочими характеристиками, начиная от низких температурных значений кристаллизации до высоких пороговых значений закипания.
- Теплоноситель не должен содержать соль, которая так “любит” выпадать в виде накипи в теплообменнике, выводя его из строя, а также разрастаться твердыми отложениями во внутреннем сечении труб.
- Необходимо, чтобы теплоноситель для отопления обладал повышенной стабильностью. Нам потребуется теплоноситель, который не распадается со временем на составные части ни под воздействием высоких температур, ни под воздействием своего химического состава. На протяжении всего срока службы, теплоноситель обязан сохранять заявленные технические характеристики, такие как: плотность, текучесть, теплоемкость, химическая инертность.
- Кроме того, теплоноситель не должен угрожать здоровью жильцов в случае протечек. Не допускаются токсичные испарения. Жидкость применяемая в отоплении должна быть полностью негорючая и не образовывать взрывоопасных газовых смесей при испарении.
- Как правило, система отопления имеет значительные объемы, таким образом одним из немаловажных критериев для рачительного домовладельца становится приемлемая стоимость теплоносителя.